Een nieuw kankervaccin heeft bemoedigende resultaten laten zien in laboratoriumstudies, die het potentieel aantonen om HPV-gerelateerde keelkanker te behandelen. Het onderzoek, gepubliceerd in Science Advances, benadrukt een unieke benadering van het ontwerpen van vaccins die de effectiviteit verder zou kunnen verbeteren dan bestaande behandelingen en inzichten zou kunnen bieden in het bouwen van betere vaccins voor andere ziekten.
De toenemende dreiging van door HPV veroorzaakte kankers
Het humaan papillomavirus (HPV) staat algemeen bekend als de oorzaak van de meeste vormen van baarmoederhalskanker, maar is ook verantwoordelijk voor een aanzienlijk en groeiend aantal andere vormen van kanker, waaronder orofaryngeale kanker (keelkanker). In de Verenigde Staten is ongeveer 70% van deze keelkankers gekoppeld aan HPV, waarbij stam 16 de voornaamste boosdoener is. Hoewel het Gardasil 9 -vaccin een HPV-infectie voorkomt, blijven de huidige behandelingsopties voor degenen bij wie reeds de diagnose HPV-gerelateerde tumoren is gesteld, beperkt tot chirurgie, bestraling en chemotherapie.
Dit is waar het nieuwe vaccin in actie komt. Het doel is niet preventie, maar behandeling – om de immuunrespons van het lichaam tegen bestaande tumoren te versterken en het risico op herhaling te verminderen.
Een slimmer vaccinontwerp: de kracht van structuur
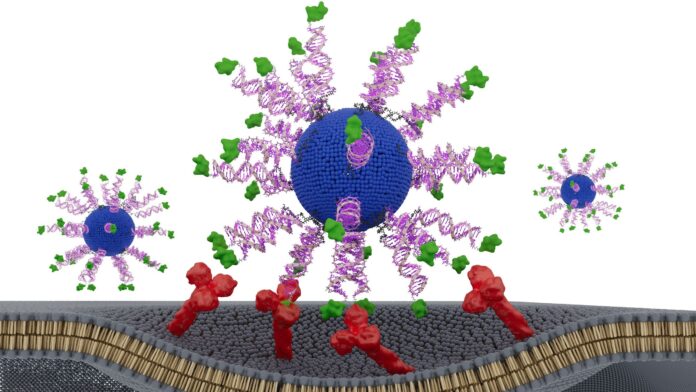
De doorbraak gaat niet alleen over wat er in het vaccin zit, maar hoe het is geregeld. Onderzoekers hebben een vaccin ontwikkeld met behulp van sferische nucleïnezuren (SNA’s) – bolvormige DNA-deeltjes die antigenen (de doeleiwitten) rechtstreeks aan immuuncellen afleveren. Dit verschilt van traditionele lineaire, op DNA gebaseerde vaccins, die minder effectief zijn bij het binnendringen van cellen.
Het team testte drie SNA-ontwerpen, waarbij alleen de manier waarop het HPV-eiwitfragment was bevestigd, varieerde. De belangrijkste bevinding: het positioneren van het fragment via zijn N-terminus (het ene uiteinde van zijn structuur) veroorzaakte de sterkste immuunrespons. Dit leidde tot tot acht keer meer productie van interferon-gamma – een cruciaal signaal voor antitumoractiviteit – waardoor dodelijke T-cellen veel effectiever werden in het vernietigen van kankercellen.
Resultaten van laboratorium- en dierstudies: een duidelijk voordeel
In laboratoriumtests met HPV-positieve hoofd- en nekkankercellen vertraagde het geoptimaliseerde vaccin de tumorgroei aanzienlijk bij muizen. Cruciaal is dat wanneer het werd getest op echte tumormonsters van patiënten, het twee tot drie keer meer kankercellen doodde vergeleken met andere ontwerpen. Het effect was niet te danken aan sterkere ingrediënten, maar aan een slimmere presentatie.
Zoals Dr. Jochen Lorch, directeur medische oncologie bij Northwestern Medicine, het verwoordde: “Het immuunsysteem is gevoelig voor de geometrie van moleculen. Door te optimaliseren hoe we het antigeen aan het SNA hechten, verwerkten de immuuncellen het efficiënter.”
Wat dit betekent voor toekomstige kankertherapieën
Hoewel er nog steeds proeven op mensen nodig zijn, suggereert dit onderzoek dat het optimaliseren van de vaccinstructuur, en niet alleen de inhoud, veel effectievere kankerbehandelingen zou kunnen opleveren. Volgens Dr. Ezra Cohen van UC San Diego Health zou dit vaccin, als het succesvol blijkt te zijn bij mensen, kunnen worden gecombineerd met bestaande therapieën om ziekten te elimineren en herhaling te voorkomen.
De implicaties reiken verder dan HPV. Uitvinder Chad Mirkin gelooft dat deze aanpak voorheen onsuccesvolle vaccinkandidaten nieuw leven zou kunnen inblazen door simpelweg hun componenten te herstructureren.
“Misschien hebben we perfect aanvaardbare vaccincomponenten laten liggen, simpelweg omdat ze in de verkeerde configuratie zaten. We kunnen daar naar teruggaan en ze herstructureren en omzetten in krachtige medicijnen.”
Deze ontdekking onderstreept het belang van precisie bij de ontwikkeling van vaccins, wat erop wijst dat zelfs kleine structurele veranderingen dramatisch betere resultaten kunnen opleveren.